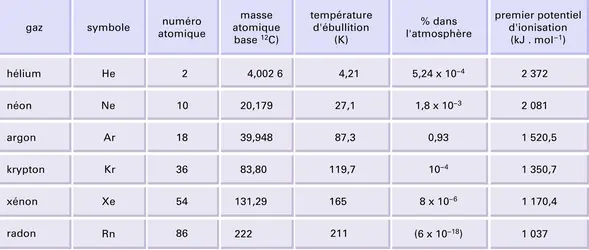
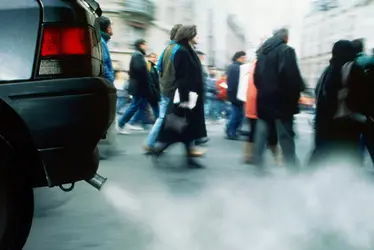gaz
Article principal
-
- Écrit par Bernard PIRE
- 3 médias
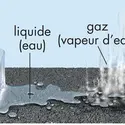
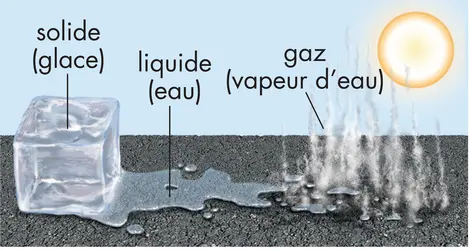
Parmi les 3 états habituels de la matière (gazeux, liquide et solide), les gaz se caractérisent par le fait qu’ils sont expansibles et compressibles. C’est pour cela qu’ils occupent totalement le volume du récipient qui les contient et qu’on peut réduire la taille de ce volume. À l’échelle microscopique, les gaz sont des ensembles désordonnés d’atomes ou de molécules, séparés par de grands espaces vides [...]
Articles associés
-
AIR - Écrit par Encyclopædia Universalis
- 2 médias
Tous les êtres vivants ont besoin d’air pour respirer. Sans air, les animaux et les plantes mourraient. L’air maintient les avions et les cerfs-volants au-dessus du sol et sert à gonfler les pneus et les ballons. La couche d’air qui entoure la Terre constitue l’atmosphère. L’air n’a pas de couleur, de goût ou d’odeur. Bien qu’il soit invisible, on peut l’entendre et le sentir sur notre peau lorsque le vent souffle [...]
-
AMMONIAC - Écrit par Bernard PIRE
- 2 médias
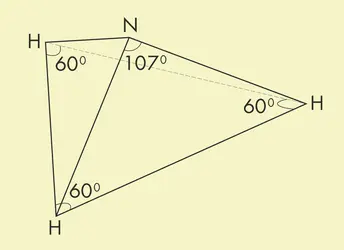
L’ ammoniac, de formule NH3, est la molécule formée par 1 atome d’azote lié à 3 atomes d’hydrogène. Sa forme est celle d’une pyramide aplatie, dont l’azote est le sommet et dont les 3 hydrogènes forment un triangle équilatéral à la base. Dans les conditions normales, c’est un gaz incolore et d’odeur piquante caractéristique. Il est irritant et dangereux, mortel à une concentration de 1 % dans l’atmosphère [...]
-
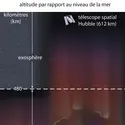
ATMOSPHÈRE - Écrit par Encyclopædia Universalis
- 1 média
L’atmosphère est la couche de gaz qui entoure la Terre. On l’appelle souvent l’air. D’autres planètes, et certains de leurs satellites les plus grands, ont aussi une atmosphère.L’atmosphère est composée de plusieurs gaz différents, maintenus près de la Terre par une force, la gravité. L’atmosphère proche de la surface est composée de 78 % d’azote et de 21 % d’oxygène environ [...]
-
AURORE POLAIRE - Écrit par Encyclopædia Universalis
- 3 médias
Les aurores polaires sont des phénomènes lumineux colorés éblouissants qui apparaissent parfois dans le ciel nocturne. Elles surviennent dans les régions de l’extrême nord et de l’extrême sud de la Terre. Dans l’hémisphère Nord, on les appelle aurores boréales. Dans l’hémisphère Sud, ce sont des aurores australes. Les aurores peuvent être de plusieurs formes, les arcs et les rayons de lumière colorée étant les plus courantes [...]
-
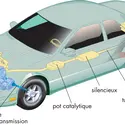
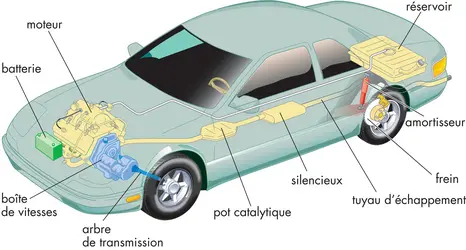
AUTOMOBILE - Écrit par Encyclopædia Universalis
- 3 médias
Il est difficile d’imaginer aujourd’hui ce qu’était la vie sans les automobiles, ou voitures. Elles facilitent les déplacements et les voyages. Elles influencent aussi l’endroit où habitent les gens, puisqu’on peut maintenant vivre loin de son travail et s’y rendre en voiture.Mais les automobiles provoquent aussi des problèmes. Dans le monde, des dizaines de milliers de personnes sont tuées ou blessées chaque année dans des accidents de la route [...]
-
AVOGADRO, Lorenzo Romano Amedeo Carlo (1776-1856)- Écrit par Bernard PIRE
- 1 média
Lorenzo Romano Amedeo Carlo Avogadro, comte de Quaregna et de Ceretto, fut un chimiste et un physicien italien du 19e siècle. Il naît le 9 août 1776 à Turin, d’un père magistrat. Il effectue des études de droit, devient juriste. Mais il abandonne sa carrière à l’âge de 30 ans, pour se consacrer aux sciences, et plus particulièrement à l’étude de l’électricité [...]
-
AZOTE - Écrit par Encyclopædia Universalis
- 1 média
L ’azote est un gaz qui constitue la majeure partie de l’ atmosphère terrestre . Cet élément chimique est aussi l’un des principaux composants de la matière des êtres vivants. L’élément azote est représenté par le symbole N en chimie. Formes de l’azote On trouve l’azote libre dans l’air et de nombreuses météorites. Les gaz que dégagent les volcans, les mines et certaines sources d’eau minérale en contiennent aussi [...]
-
BALLON - Écrit par Encyclopædia Universalis
- 1 média
Comme les dirigeables, les ballons sont des aérostats, des appareils plus légers que l’air. Ils sont remplis de gaz ou d’air chaud, ce qui leur permet de flotter dans l’air. Grâce aux premières expériences de vol en ballon, on a pu mettre au point des dirigeables à moteur, puis des avions. Types de ballons Les ballons peuvent être de toutes tailles et de toutes formes : aussi petits qu’un jouet ou assez grands pour transporter des passagers [...]
-
BEC BUNSEN - Écrit par Bernard PIRE
- 3 médias
L’appareil de laboratoire appelé « bec Bunsen » est un brûleur à gaz du nom du chimiste allemand Robert Bunsen, qui contribua à son invention en 1855, plus particulièrement avec un de ses assistants à l’université d’Heidelberg, Peter Desdega. Le bec Bunsen est couramment utilisé dans des laboratoires de chimie et de biologie. Il a la forme d’une petite cheminée alimentée par une arrivée latérale [...]
-
BULLE ,physique - Écrit par Bernard PIRE
- 3 médias
Les bulles font partie de notre quotidien : bulles de savon, bulles dans une boisson pétillante, bulles dans le sillage d’un bateau... Les bulles contiennent une petite quantité de gaz : de l’air dans une bulle de savon, du gaz carbonique (dioxyde de carbone, CO2) dans une boisson pétillante. Dans le cas des bulles de savon en suspension dans l’air, le gaz intérieur est séparé de l’extérieur par une fine paroi de liquide [...]
-
CHLORE - Écrit par Bernard PIRE
- 2 médias
L’ élément chlore, de symbole Cl et de numéro atomique 17, est un halogène (comme le fluor, le brome, l’iode ou l’astate). Il est présent dans la nature sous la forme de 2 isotopes stables : le chlore 35, dont le noyau contient 18 neutrons, et le chlore 37, dont le noyau en contient 20. Il se liquéfie facilement, à la température de – 35 0C à pression normale, à une température plus élevée sous pression [...]
-
DILATATION ET CONTRACTION ,sciences - Écrit par Bernard PIRE
- 1 média
La dilatation d’un corps est son augmentation de volume. La contraction traduit au contraire une diminution de ce volume. Généralement, un corps se dilate lorsqu’on élève sa température. Réciproquement, il se contracte lorsque la température baisse. Cela est vrai pour la plupart des corps solides, liquides ou gazeux. La raison principale est que l’échauffement accroît l’énergie de mouvement des molécules ou des atomes [...]
-
DIRIGEABLE - Écrit par Encyclopædia Universalis
- 1 média
Un dirigeable est une sorte de ballon ascensionnel. Comme lui, il est rempli d’un gaz plus léger que l’air qui lui permet de flotter dans l’air. Mais, contrairement à lui, il possède un système de propulsion, et est dirigé par un gouvernail. C’est d’ailleurs du verbe « diriger » que vient son nom. La plupart des dirigeables ont la forme d’un long cigare [...]
-
ÉTOILE - Écrit par Encyclopædia Universalis
- 5 médias
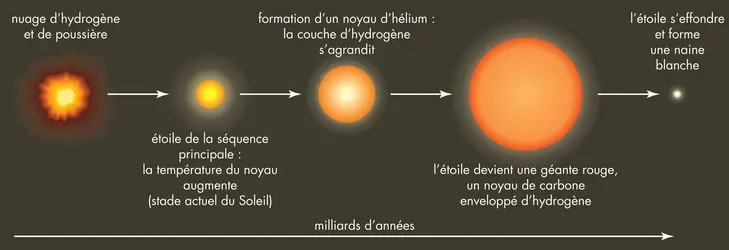
Les étoiles sont de grandes masses de gaz brillantes. Le Soleil est l’étoile la plus proche de la Terre. La plupart des lumières qui brillent dans le ciel nocturne sont des étoiles. Une infinité d’autres étoiles sont trop éloignées de la Terre pour être vues sans télescope.Les étoiles forment de grands groupes, les galaxies. Le Soleil et son système solaire, dans lequel se trouve la Terre, font partie de la Voie lactée [...]
-
FLUOR - Écrit par Bernard PIRE
- 4 médias
Le fluor, de symbole F et de numéro atomique 9, est le premier élément chimique de la colonne des halogènes (la 17e dans le tableau périodique des éléments, laquelle comprend aussi le chlore, le brome, l’iode et l’astate). Le noyau atomique du fluor contient 9 protons et 10 neutrons. Il est entouré de 9 électrons lorsqu’il n’est pas ionisé [...]
-
FROID ,physique - Écrit par Bernard PIRE
- 3 médias
Le froid, sensation contraire au chaud, est caractérisé en physique par une température très basse, qui correspond à un état de très faible agitation moléculaire. Les mouvements entre les molécules sont ralentis avec le froid. Les températures les plus basses atteintes naturellement sur la Terre sont de l’ordre de – 60 0C. Le froid amène les gaz à se liquéfier et les liquides à se solidifier [...]
-
HÉLIUM - Écrit par Bernard PIRE
- 1 média
L’ hélium, de symbole He et de numéro atomique 2, est, à température ordinaire, un gaz inodore, incolore, 7 fois plus léger que l’air. Son atome possède 2 électrons et il ne se lie pratiquement pas avec les autres atomes ; il a donc une grande inertie chimique (absence de réaction chimique avec une autre substance). Classé dans les gaz nobles, l’hélium est présent sous la forme de 2 isotopes [...]
-
HYDROGÈNE - Écrit par Encyclopædia Universalis
L’ hydrogène est l’élément chimique le plus simple et le plus abondant dans l’Univers. L’élément hydrogène est représenté par le symbole H en chimie. Formes de l’hydrogène L’hydrogène représente moins de 1 % de la croûte terrestre et il est rare dans notre atmosphère. Mais, associé à l’oxygène, il est le principal constituant de l’eau qui circule sur notre planète, jusque dans les tissus des végétaux, des animaux et des hommes [...]
-
JUPITER ,planète - Écrit par Encyclopædia Universalis
- 2 médias
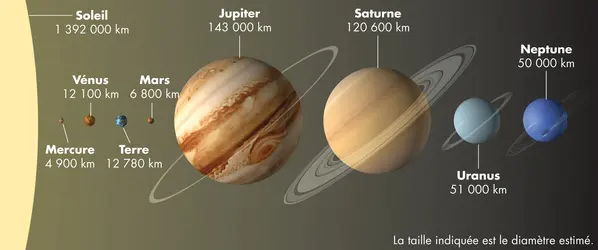
Jupiter est l’une des planètes qui gravitent (tournent) autour du Soleil. C’est la plus grosse planète du système solaire. Elle orbite autour du Soleil à une distance moyenne de 778 millions de kilomètres : c’est la 5e planète à partir de cet astre.StructureJupiter est si grosse qu’elle pourrait contenir plus de 1 000 planètes Terre. Son diamètre est d’environ 143 000 kilomètres [...]
-
MATIÈRE - Écrit par Encyclopædia Universalis
- 1 média
Tout ce qui occupe de l’espace, comme l’air, l’eau, les rochers et même les personnes, est de la matière. Les différentes matières peuvent être décrites par leur masse, ou la quantité de matériau qui les compose. Une boule de bowling, par exemple, a une masse plus importante qu’un ballon de plage. États de la matière La matière existe sous plusieurs formes, ou états [...]
-
NÉON - Écrit par Bernard PIRE
- 2 médias
Le néon est l’ élément chimique de symbole Ne et de numéro atomique 10. Son noyau contient par conséquent 10 protons et est entouré de 10 électrons. Le noyau de l’isotope le plus commun contient aussi 10 neutrons. Comme l’hélium, l'argon, le krypton, le xénon et le radon, le néon appartient à la famille des gaz rares, parfois appelés gaz nobles, qui sont caractérisés par une très grande inertie chimique [...]
-
OHM LOI D'- Écrit par Bernard PIRE
- 1 média
En électricité, la loi d’Ohm permet de calculer la différence de potentiel (ou tension) U entre les extrémités d’un conducteur de résistance R traversé par un courant électrique continu d’ intensité I, grâce à la formule U = RI. U se mesure en volts, R en ohms et I en ampères. Cette loi a été établie en 1827 par le physicien allemand Georg Simon Ohm [...]
-
OXYGÈNE - Écrit par Encyclopædia Universalis
- 1 média
L’ oxygène est l’élément chimique le plus fréquent sur Terre. C’est l’un des principaux constituants de l’air, et il est nécessaire à la vie des plantes, des animaux et des hommes. L’élément oxygène est représenté par le symbole O en chimie. L’ oxygène constitue environ 20 % de l’atmosphère et 90 % (en poids) de l’eau. Il représente près de 50 % des roches et du sable présents dans la croûte terrestre [...]
-
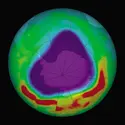
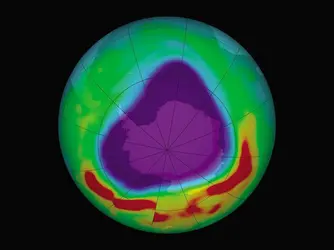
OZONE - Écrit par Encyclopædia Universalis
- 2 médias
Gaz bleu pâle, d’odeur forte et dangereux à respirer, l’ozone est une forme d’ oxygène dont la molécule comporte 3 atomes au lieu de 2. La formule scientifique de l’ozone est O3. L’ozone est souvent produit lorsqu’une charge électrique, comme l’éclair, passe dans l’air. On remarque parfois son odeur désagréable après un orage ou autour d’un équipement électrique [...]
-
PLANÈTE - Écrit par Encyclopædia Universalis
- 2 médias
Les planètes sont de gros objets naturels gravitant autour d’une étoile. Huit planètes tournent autour du Soleil. De la plus proche à la plus lointaine du soleil, ce sont Mercure, Vénus, la Terre, Mars, Jupiter, Saturne, Uranus et Neptune. Le système solaire est constitué du Soleil et de tous les objets tournant autour de lui, dont les 8 planètes [...]
-
POLLUTION ATMOSPHÉRIQUE - Écrit par Mélanie PEREZ
- 2 médias
L’ air que nous respirons peut être contaminé par différents types de polluants (gaz, particules, produits chimiques...). Les gaz d’échappement des véhicules, les fumées noires sortant des usines ou encore le smog (brouillard qui s’installe au-dessus des grandes villes industrialisées du monde) constituent la partie visible de la pollution de l’air [...]
-
QUALITÉ DE L'AIR - Écrit par Mélanie PEREZ
L'air que nous respirons est un mélange de gaz. Il est composé de 78 % de diazote (N2), de 21 % de dioxygène (O2) et de 0,95 % d'argon. Cet air peut être pollué par des substances gazeuses, liquides ou solides.Les substances qui viennent perturber la qualité de l’airLes substances responsables de la pollution de l’air peuvent être d'origine naturelle (matériaux rejetés par les volcans, dioxyde de carbone produit par les plantes [...]
Documents
Les fluorures naturels
Où trouve-t-on le fluor ? [...]
Le fluor et la santé
Le fluor est utilisé en thérapeutique. [...]
Action physiologique du fluor
Le fluor présente une très grande toxicité. [...]
La dilatation des océans
Avec le réchauffement climatique, de la fonte des glaces et de la dilatation de l’eau due à l’élévation de température, quel est le facteur le plus impliqué dans la montée du niveau marin ? [...]
Le « sel ammoniac »
Le sel ammoniac est connu depuis l’Antiquité, mais ce n’est qu’au 18e siècle que l’ammoniac put être isolé. [...]
Le sel de table, ou chlorure de sodium
Le sel (NaCl), ou chlorure de sodium, est un des produits les plus nécessaires à la vie. [...]
Dan Flavin : néon et art contemporain
Artiste américain appartenant au mouvement de l’art minimal du 20e siècle, Dan Flavin a réalisé ses œuvres avec un matériau aussi inattendu que typiquement moderne : le tube fluorescent.… [...]