chimie minérale
Article principal
-
- Écrit par Bernard PIRE
La chimie minérale est la science qui décrit les corps simples et les composés de tous les éléments autres que le carbone, et de quelques molécules très simples contenant un seul atome de carbone (oxydes de carbone, carbonates, cyanures...). On parle de chimie minérale car, à l’origine, les corps étudiés provenaient du règne minéral. On l’appelle parfois chimie inorganique, par opposition à la [...]
Articles associés
-
ACIDE CHLORHYDRIQUE - Écrit par Bernard PIRE
- 3 médias
L’ acide chlorhydrique, parfois appelé esprit de sel, est du chlorure d’hydrogène en solution. Le chlorure d’hydrogène, de formule moléculaire HCl, qui est un gaz d’odeur forte et étouffante, est en effet très soluble dans l’eau, qui peut en dissoudre plusieurs centaines de fois son volume. En solution dans l’eau, le liquide est incolore et très corrosif [...]
-
ALUMINIUM - Écrit par Bernard PIRE
- 3 médias
L’ aluminium, de symbole Al et de numéro atomique 13, est un métal peu dense, de couleur blanche. Il s’oxyde facilement en se recouvrant d’une fine couche d’ alumine (Al2O3) qui le protège d’une corrosion plus importante. L’aluminium est un bon conducteur électrique, mais l’alumine est un isolant. L'aluminium est un des éléments les plus abondants dans la croûte terrestre, après l’oxygène et le [...]
-
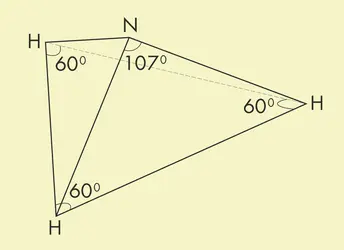
AMMONIAC - Écrit par Bernard PIRE
- 2 médias
L’ ammoniac, de formule NH3, est la molécule formée par 1 atome d’azote lié à 3 atomes d’hydrogène. Sa forme est celle d’une pyramide aplatie, dont l’azote est le sommet et dont les 3 hydrogènes forment un triangle équilatéral à la base. Dans les conditions normales, c’est un gaz incolore et d’odeur piquante caractéristique. Il est irritant et dangereux, mortel à une concentration de 1 % dans l’atmosphère [...]
-
ARGENT ,métal - Écrit par Bernard PIRE
- 2 médias
L’ argent (symbole Ag) est un élément chimique, classé parmi les métaux, de numéro atomique 47. Il possède 2 isotopes stables (107Ag et 109Ag), presque également abondants dans la nature, et de nombreux isotopes radioactifs. Les minerais d’argent sont rares et répartis sur toute la Terre. Le principal minerai est l’argentite (Ag2S), un minerai sulfuré exploité en Amérique du Sud et au Mexique [...]
-
AZOTE - Écrit par Encyclopædia Universalis
- 1 média
L ’azote est un gaz qui constitue la majeure partie de l’ atmosphère terrestre . Cet élément chimique est aussi l’un des principaux composants de la matière des êtres vivants. L’élément azote est représenté par le symbole N en chimie. Formes de l’azote On trouve l’azote libre dans l’air et de nombreuses météorites. Les gaz que dégagent les volcans, les mines et certaines sources d’eau minérale en contiennent aussi [...]
-
CHLORE - Écrit par Bernard PIRE
- 2 médias
L’ élément chlore, de symbole Cl et de numéro atomique 17, est un halogène (comme le fluor, le brome, l’iode ou l’astate). Il est présent dans la nature sous la forme de 2 isotopes stables : le chlore 35, dont le noyau contient 18 neutrons, et le chlore 37, dont le noyau en contient 20. Il se liquéfie facilement, à la température de – 35 0C à pression normale, à une température plus élevée sous pression [...]
-
COBALT - Écrit par Encyclopædia Universalis
- 1 média
Le cobalt, de symbole Co et de numéro atomique 27, est un élément chimique métallique du même groupe que le fer (Fe) et le nickel (Ni). Sa masse atomique est de 59. Pendant des siècles, il a été utilisé pour colorer les vernis et les céramiques d’un bleu profond. Aujourd’hui, il est mélangé avec d’autres métaux pour produire des alliages industriels [...]
-
CUIVRE - Écrit par Bernard PIRE
- 7 médias
Le cuivre est un métal utilisé et travaillé depuis des millénaires par les hommes, soit à l’état pur, soit sous forme d’alliages (les plus importants étant le laiton et le bronze). Ses propriétés électriques en font un élément indispensable à la société industrielle. L’ élément chimique cuivre a pour symbole Cu et son numéro atomique est 29. Il se cristallise dans un système cubique à faces centrées [...]
-
FLUOR - Écrit par Bernard PIRE
- 4 médias
Le fluor, de symbole F et de numéro atomique 9, est le premier élément chimique de la colonne des halogènes (la 17e dans le tableau périodique des éléments, laquelle comprend aussi le chlore, le brome, l’iode et l’astate). Le noyau atomique du fluor contient 9 protons et 10 neutrons. Il est entouré de 9 électrons lorsqu’il n’est pas ionisé [...]
-
HÉLIUM - Écrit par Bernard PIRE
- 1 média
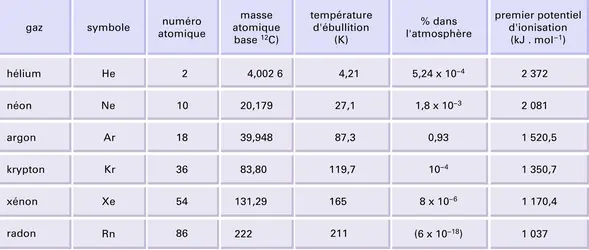
L’ hélium, de symbole He et de numéro atomique 2, est, à température ordinaire, un gaz inodore, incolore, 7 fois plus léger que l’air. Son atome possède 2 électrons et il ne se lie pratiquement pas avec les autres atomes ; il a donc une grande inertie chimique (absence de réaction chimique avec une autre substance). Classé dans les gaz nobles, l’hélium est présent sous la forme de 2 isotopes [...]
-
HYDROGÈNE - Écrit par Encyclopædia Universalis
L’ hydrogène est l’élément chimique le plus simple et le plus abondant dans l’Univers. L’élément hydrogène est représenté par le symbole H en chimie. Formes de l’hydrogène L’hydrogène représente moins de 1 % de la croûte terrestre et il est rare dans notre atmosphère. Mais, associé à l’oxygène, il est le principal constituant de l’eau qui circule sur notre planète, jusque dans les tissus des végétaux, des animaux et des hommes [...]
-
NÉON - Écrit par Bernard PIRE
- 2 médias
Le néon est l’ élément chimique de symbole Ne et de numéro atomique 10. Son noyau contient par conséquent 10 protons et est entouré de 10 électrons. Le noyau de l’isotope le plus commun contient aussi 10 neutrons. Comme l’hélium, l'argon, le krypton, le xénon et le radon, le néon appartient à la famille des gaz rares, parfois appelés gaz nobles, qui sont caractérisés par une très grande inertie chimique [...]
-
OR - Écrit par Bernard PIRE
- 6 médias
L’or, de symbole Au (du latin aurum) et de numéro atomique 79, est un métal précieux travaillé par l’homme depuis la plus haute antiquité. Sa densité est de 19,5. L’or est le plus malléable et le plus ductile de tous les métaux. On peut en faire des feuilles d’une épaisseur inférieure au dixième de nanomètre et des fils d’une section minuscule : 1 gramme d’or peut être étiré en un fil de plusieurs kilomètres de longueur [...]
-
OXYGÈNE - Écrit par Encyclopædia Universalis
- 1 média
L’ oxygène est l’élément chimique le plus fréquent sur Terre. C’est l’un des principaux constituants de l’air, et il est nécessaire à la vie des plantes, des animaux et des hommes. L’élément oxygène est représenté par le symbole O en chimie. L’ oxygène constitue environ 20 % de l’atmosphère et 90 % (en poids) de l’eau. Il représente près de 50 % des roches et du sable présents dans la croûte terrestre [...]
-
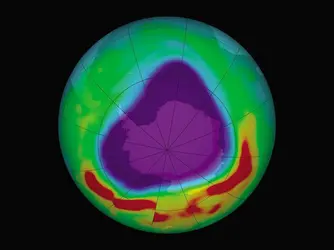
OZONE - Écrit par Encyclopædia Universalis
- 2 médias
Gaz bleu pâle, d’odeur forte et dangereux à respirer, l’ozone est une forme d’ oxygène dont la molécule comporte 3 atomes au lieu de 2. La formule scientifique de l’ozone est O3. L’ozone est souvent produit lorsqu’une charge électrique, comme l’éclair, passe dans l’air. On remarque parfois son odeur désagréable après un orage ou autour d’un équipement électrique [...]
-
PLUTONIUM - Écrit par Bernard PIRE
- 1 média
Le plutonium est un élément transuranien (de numéro atomique supérieur à celui de l’uranium, c’est-à-dire 92), de symbole Pu, de numéro atomique 94. Le plutonium a été produit et découvert en 1940 par l’équipe de physiciens nucléaires de l’université de Californie à Berkeley, conduite par Glenn T. Seaborg (qui a reçu le prix Nobel de chimie en 1951 pour cette découverte) [...]
-
URANIUM - Écrit par Encyclopædia Universalis
- 1 média
L’ uranium est un élément chimique utilisé pour créer de l’énergie nucléaire à usage civil ou militaire. Il est radioactif, c’est-à-dire qu’il dégage de l’énergie sous forme de minuscules particules. L’élément uranium est représenté par le symbole U en chimie. Répartition géographique On trouve de l’uranium en de nombreux points de l’écorce terrestre [...]
-
ZINC - Écrit par Bernard PIRE
- 4 médias
Le zinc, de symbole Zn et de numéro atomique 30, est un métal blanc bleuâtre utilisé couramment. Sa densité est de 7,13 et sa température de fusion de 420 0C environ. Il est cassant à froid, mais il est ductile au-dessus de 100 0C. Un échantillon de zinc laissé à l’air libre se couvre d’une mince couche d’hydrocarbonate de zinc, qui joue un rôle protecteur contre l’oxydation [...]
Documents
La bauxite
La bauxite est le minerai d’aluminium le plus commun. [...]
Histoire de l’obtention de l’aluminium
L’alun, déjà décrit par Pline l’Ancien, est le plus anciennement connu des composés d’aluminium. Mais ce n’est qu’au 19e siècle que l’élément sera isolé. [...]
Le sel de table, ou chlorure de sodium
Le sel (NaCl), ou chlorure de sodium, est un des produits les plus nécessaires à la vie. [...]
Les fluorures naturels
Où trouve-t-on le fluor ? [...]
Le fluor et la santé
Le fluor est utilisé en thérapeutique. [...]
Action physiologique du fluor
Le fluor présente une très grande toxicité. [...]
Le combustible nucléaire MOX
Le MOX (Mixed Oxide) désigne un combustible constitué d’un mélange d’oxydes de plutonium et d’uranium, utilisé actuellement dans certains réacteurs à eau et uranium enrichi. [...]
Le « sel ammoniac »
Le sel ammoniac est connu depuis l’Antiquité, mais ce n’est qu’au 18e siècle que l’ammoniac put être isolé. [...]
Dan Flavin : néon et art contemporain
Artiste américain appartenant au mouvement de l’art minimal du 20e siècle, Dan Flavin a réalisé ses œuvres avec un matériau aussi inattendu que typiquement moderne : le tube fluorescent.… [...]
L’argentite
L’argentite est le minerai principal des gisements d’argent (d’où son nom). Elle peut contenir jusqu’à 87 % de cet élément natif. [...]